Charlotte Maurin, Suzanne Atkinson, Linda Hamouche et Jean-François BussièresComment citer cet article: Maurin C, Atkinson S, Hamouche L, Bussières JF. Incidents et accidents médicamenteux en établissement de santé: une analyse descriptive au sein d’un CHU mère-enfant de 2018 à 2022. Can J Hosp Pharm. 2024;77(1):e3528. doi: 10.4212/cjhp.3528
RÉSUMÉ
Contexte
La sécurité des soins prodigués repose notamment sur une analyse des incidents et accidents médicamenteux (IAM).
Objectif
L’objectif principal est de décrire les IAM au sein d’un centre hospitalier universitaire (CHU).
Méthodologie
Cette étude descriptive rétrospective utilisait les déclarations provenant d’un CHU mère-enfant de 500 lits. Tous les incidents et accidents (IA) déclarés entre le 1er avril 2018 et le 31 mars 2022 ont été considérés. Ont été inclus tous les IAM survenus durant une admission ou en ambulatoire. Certaines variables ont été recodées manuellement. Des statistiques descriptives ont été effectuées.
Résultats
Un total de 23 284 IA ont été considérés, incluant 7578 IAM. Il y avait une moyenne de 15,9 ± 14,0 IA déclarés par jour et 5,2 ± 0,3 IAM par jour. Il y avait 22,4 IAM/1000 jours-présence. La majorité des IAM sont survenus en chirurgie (20 %, 1530/7578), en oncologie (19 %, 1405/7578) et en pédiatrie (16 %, 1200/7578). La majorité était associée à une mauvaise posologie (21 %, 1575/7578), à des infiltrations/extravasations/voies retirées (19 %, 1405/7578) et à des omissions (16 %, 1205/7578). Des conséquences physiques ont été déclarées dans 15 % (1158/7578) des IAM. En revanche, des conséquences psychologiques ont été déclarées pour moins de 1 % (44/7578) des IAM.
Conclusions
L’étude offre un profil descriptif complet sur quatre ans. La majorité des IA rapportés n’ont pas mené à des conséquences pour les patients. Le partage de ratios favorise l’analyse comparative avec d’autres établissements et peut contribuer aux échanges entourant la réduction des risques. Une culture de déclaration des événements est présente au sein de l’établissement.
Mots-clés: gestion des risques, incidents, accidents, médicaments, prévention
ABSTRACT
Background
The safety of care provided is based on an analysis of medication incidents and accidents.
Objective
The primary objective was to describe medication-related incidents and accidents (I&A) within a university-affiliated hospital.
Methods
This retrospective descriptive study was based on data from a 500-bed mother-child university-affiliated hospital. All I&As declared between April 1, 2018, and March 31, 2022, were considered. The analysis included all medication-related I&As that occurred during an admission or in an outpatient setting. Some variables were recoded manually. Descriptive statistical analyses were performed.
Results
A total of 23 284 I&As were considered, including 7578 medication-related I&As. Daily averages of 15.9 ± 14.0 I&As and 5.2 ± 0.3 medication-related I&As were reported. There were 22.4 medication-related I&As/1000 inpatient days. The majority of medication-related I&As occurred in surgery (20%, 1530/7578), oncology (19%, 1405/7578), and pediatrics (16%, 1200/7578). Most were associated with incorrect dosing (21%, 1575/7578); infiltration, extravasation, or removed lines (19%, 1405/7578); and omissions (16%, 1205/7578). Physical consequences were reported in 15% (1158/7578) of the medication-related I&As. Conversely, psychological consequences were reported in less than 1% (44/7578) of medication-related I&As.
Conclusions
This study provides a comprehensive descriptive profile over a 4-year period. Most of the reported I&As did not lead to consequences for patients. The sharing of ratios promotes comparative analysis with other facilities and can contribute to discussions about risk reduction. A culture of reporting events is present within this health care facility.
Keywords: risk management, incidents, accidents, medications, prevention
En 2017, l’Organisation mondiale de la santé (OMS) a proposé l’initiative « les médicaments sans les méfaits »1. On rapporte que le coût annuel associé aux incidents et accidents (IA) médicamenteux (IAM) a été estimé à 42 milliards de dollars aux États-Unis par an.
Selon le ministère de la santé et des services sociaux du Québec (MSSS), un incident est « une action ou une situation qui n’entraîne pas de conséquence sur l’état de santé ou le bien-être d’un usager […], mais dont le résultat est inhabituel et qui, en d’autres occasions, pourraient entrainer des conséquences ». De plus, un accident est une « action ou situation où le risque se réalise et est, ou pourrait être, à l’origine de conséquences sur l’état de santé ou le bien-être de l’usager »2.
Les IA peuvent inclure ou porter notamment sur les chutes, les médicaments, les traitements, les diètes, les tests diagnostiques, le matériel, les équipements, les bâtiments, les effets personnels, les abus et les agressions2. Ainsi, les IAM peuvent survenir en milieu hospitalier et communautaire ainsi qu’à toutes les étapes du circuit du médicament3.
Afin de réduire les risques associés aux IA, le Québec s’est doté d’un encadrement juridique entourant la déclaration et la prévention depuis 2002. Ce cadre juridique repose sur la Loi sur les services de santé et services sociaux4, sur le cadre de référence du registre national des IA5, des lignes directrices6 et un guide d’utilisation du rapport de déclaration des IA2.
L’ensemble des IA sont déclarés localement par le personnel soignant au moyen d’un formulaire papier, puis saisis dans le système d’information sur la sécurité des soins et des services (SISSS). Par la suite, les données locales sont traitées de façon centralisée afin d’alimenter un registre national d’IA. Un rapport synthèse, par exercice financier, des IA survenus est publié annuellement par le MSSS5.
En vertu de ce cadre juridique, chaque établissement de santé doit se doter d’un comité de gestion des risques4. Le comité doit rechercher des moyens permettant l’identification et l’analyse des risques d’IA, les développer et en faire la promotion. Il doit également mettre en place un système de surveillance qui comprend un registre local et faire des recommandations au Conseil d’administration de l’établissement.
Dans notre établissement, nous procédons périodiquement à l’analyse des déclarations d’IAM. Des travaux précédents ont été publiés sur le nombre total d’IA (IAT) et le nombre d’IAM de notre établissement de 2004 à 2010 et de 2011 à 20187,8.
Il s’agit d’une étude descriptive rétrospective.
L’objectif principal est de décrire les IAM au sein d’un centre hospitalier universitaire (CHU).
L’étude se déroule dans un CHU mère-enfant de 500 lits.
Compte tenu du caractère transversal du circuit du médicament, le pharmacien gestionnaire de risque est appelé à analyser l’ensemble des IAM. Le projet a été soumis au comité d’éthique de la recherche.
Tous les IA déclarés entre le 1er avril 2018 et le 31 mars 2022 ont été considérés. Chaque IA est codifié selon un guide d’utilisation2.
Toutes les doses dispensées de médicaments ont été extraites de l’application logistique (GRM Espresso, Logibec).
Le nombre d’IAT a été extrait par exercice financier (c.-à-d. 2018–2019, 2019–2020, 2020–2021, 2021–2022). Par la suite, tous les IAM ont été extraits dans un chiffrier (MS Excel). Lorsque le rapport d’IA est rempli par le personnel soignant, celui-ci doit codifier le type d’événement. Un événement de type B se rapporte à un médicament, un traitement/une intervention ou une diète. Les variables suivantes ont été extraites pour chaque IAM : numéro unique, date de l’événement, titre d’emploi du déclarant, lieu où l’IAM est survenu, type d’événement (médication ou traitement), circonstance, gravité (A – circonstance ou situation à risque de provoquer un événement indésirable ou d’avoir des conséquences pour l’usager; B – un événement indésirable est survenu mais l’usager n’a pas été touché; de C à I, les énoncés débutent par « un événement indésirable qui est survenu et a touché l’usager » suivi des descriptifs ci-après ; C – … sans lui causer de conséquence, D – … et des vérifications additionnelles ont dû être faites pour vérifier la présence ou l’apparition de conséquences, E1 – … et est à l’origine de conséquences mineures et temporaires n’exigeant que des interventions non spécialisées sans hospitalisation ou prolongation d’hospitalisation, E2 – … et est à l’origine de conséquences temporaires nécessitant des soins, services, interventions ou traitements spécialisés qui vont au-delà des services courants mais qui n’ont aucun impact sur la nécessité/durée de l’hospitalisation ou de l’épisode de soins, F – … et est à l’origine de conséquences temporaires exigeant des soins/traitements supplémentaires spécialisés et qui ont un impact sur la nécessité/durée de l’hospitalisation ou de l’hébergement, G – … et est à l’origine de conséquences permanentes sur ses fonctions physiologiques, motrices, sensorielles, cognitives ou psychologiques, H – … et est à l’origine de conséquences nécessitant des interventions de maintien de la vie, I – … et est à l’origine de conséquences qui ont contribué à son décès), âge et sexe de la personne touchée, conséquences, date de saisie, état de la divulgation, quart de travail, fonction du déclarant, description de l’événement et médicament(s) impliqué(s), étape du circuit du médicament, événement sentinelle (oui/non). Les données ont été extraites par une assistante de recherche (CM).
Ont été inclus tous les IAM survenus durant une admission ou en ambulatoire. Ont été exclus tous les IAM survenus dans les écoles associées à notre établissement, ou survenus au domicile ou encore tous les IAM liés à l’utilisation de matériel médical, de gaz médicaux, de médicaments dérivés du sang, d’allergènes ou de tests allergologiques, de nutrition entérale, de laits maternels, de radioisotopes et de tests diagnostiques. Afin de bonifier notre analyse, certaines variables ont été recodées manuellement9,10.
Étant donné que certains formats de médicaments permettent de dispenser plus d’une dose, un facteur de correction a été appliqué à certains formats (soit, insuline fiole/cartouche (3×), inhalateur de salbutamol (200×)). Dans certains cas, le facteur de correction a été établi à partir de la dose usuelle adulte (p. ex., céfazoline 10 g permet 10 doses de 1 g). Ainsi, des facteurs de correction ont été appliqués à certains formats de céfazoline, pipéracilline-tazobactam, ceftriaxone, vancomycine et diphenhydramine.
Dans un premier temps, un profil des IA a été préparé. Ce profil comprend le nombre d’IAT, par jour, par 100 admissions, par 1000 jours-présence (JP) et par 1000 doses dispensées. Il comprend également la proportion selon le sexe, l’âge moyen, le nombre (%) d’IAM par quart de travail et le nombre (%) selon la gravité. Dans un deuxième temps, un profil du nombre d’IAM et de JP par clientèle en ordre décroissant a été calculé. Dans un troisième temps, un profil du nombre d’IAM par circonstance en ordre décroissant a été calculé. Dans un quatrième temps, un profil du nombre d’IAM par 1000 doses dispensées en ordre décroissant pour une sélection de 25 médicaments a été calculé. Les ratios par 1000 doses dispensées ont été calculés pour les médicaments impliqués dans un nombre minimal d’IAM de 25.
Des statistiques descriptives ont été effectuées.
Les résultats de cette étude et d’autres travaux complémentaires ont été présentés à un panel d’experts en avril 2023 afin de discuter des résultats et d’identifier des pistes d’amélioration.
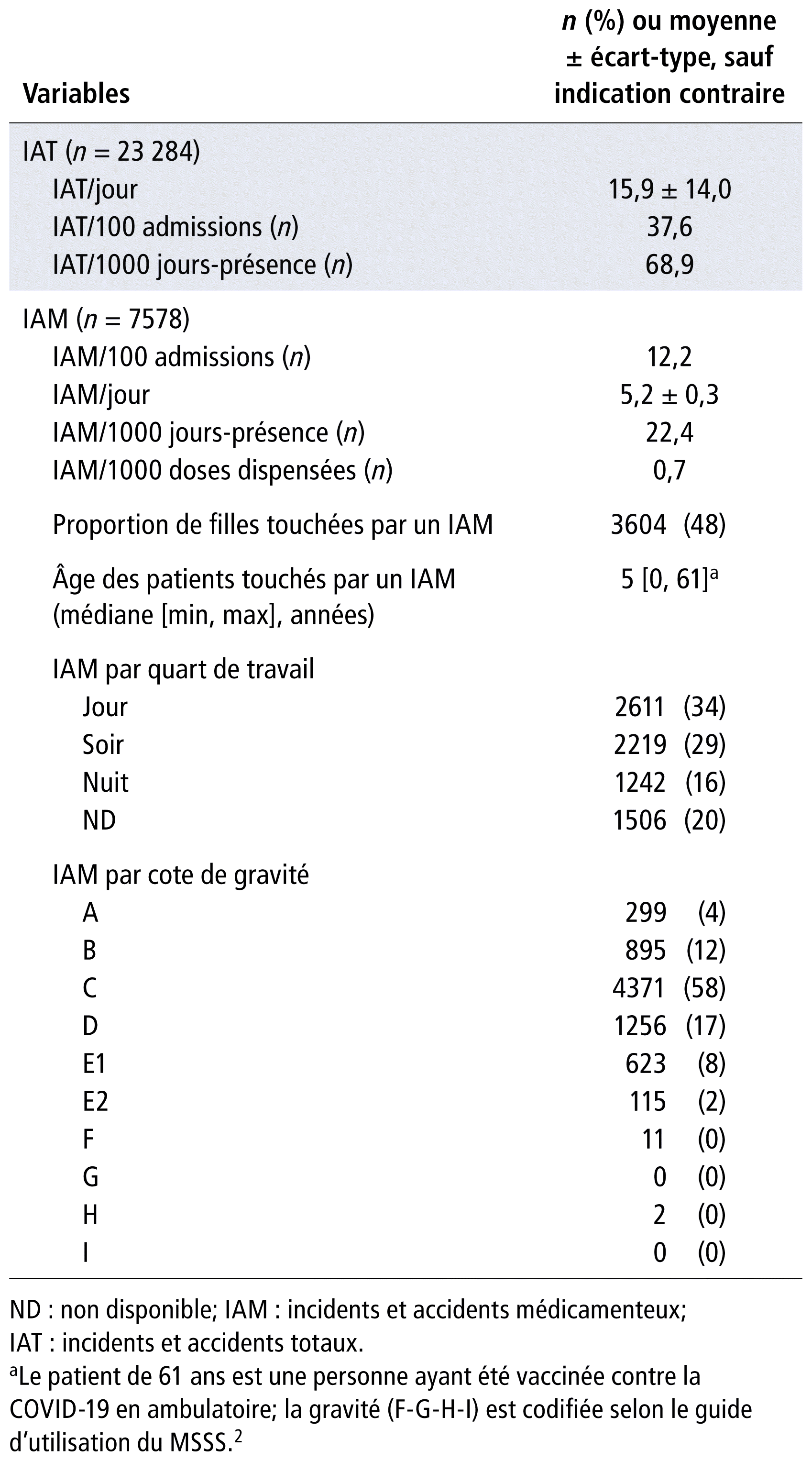
Du 1er avril 2018 au 31 mars 2022, un 23 284 IAT ont été considérés et 7578 IAM (33 %) ont été analysés (tableau 1). Il y avait 5550 IAT et 1875 IAM en 2018–2019, 5739 IAT et 1737 IAM en 2019–2020, 6062 IAT et 1989 IAM en 2020–2021 et 5933 IAT et 1977 IAM en 2021–2022.
TABLEAU 1 Profil des incidents et accidents

Les rapports d’IAM étaient rédigés par les déclarants suivants : infirmier(ière) (81 %, 6113/7578), assistant(e) infirmière chef (6 %, 451/7578), candidat à l’exercice de la profession d’infirmière (5 %, 366/7578), médecin (1 %, 85/7578), et autres (7 %, 563/7578).
En ce qui concerne les événements de gravité F à I (n=13), 11 événements (gravité F) ont entraîné des conséquences temporaires et un impact sur la nécessité ou la durée de l’hospitalisation; pour ces cas, la circonstance était principalement (55 %, 6/11) la survenue d’une infiltration/extravasation/voie retirée. Les autres circonstances étaient une mauvaise posologie (2/11), un mauvais médicament (1/11), une omission (1/11), une mauvaise identification de l’usager (1/11). De plus, deux évènements ont été à l’origine de conséquences nécessitant des interventions de maintien de la vie (gravité H). Dans un cas, le non-respect d’une procédure/protocole/ordonnance (soit, un protocole de surveillance des opiacés incorrectement suivi) a été associé à une détresse respiratoire survenue à la suite de l’administration de morphine. Dans l’autre cas, l’administration d’un mauvais médicament (soit, l’administration rapide de vancomycine par erreur à la suite d’une dilution du médicament dans une fiole de NaCl non identifiée) est survenue. Au total, 0,3 % (21/7578) ont été codés comme événement sentinelle.
L’étape du circuit du médicament n’était pas renseignée pour 33 % (2513/7578) des IAM.
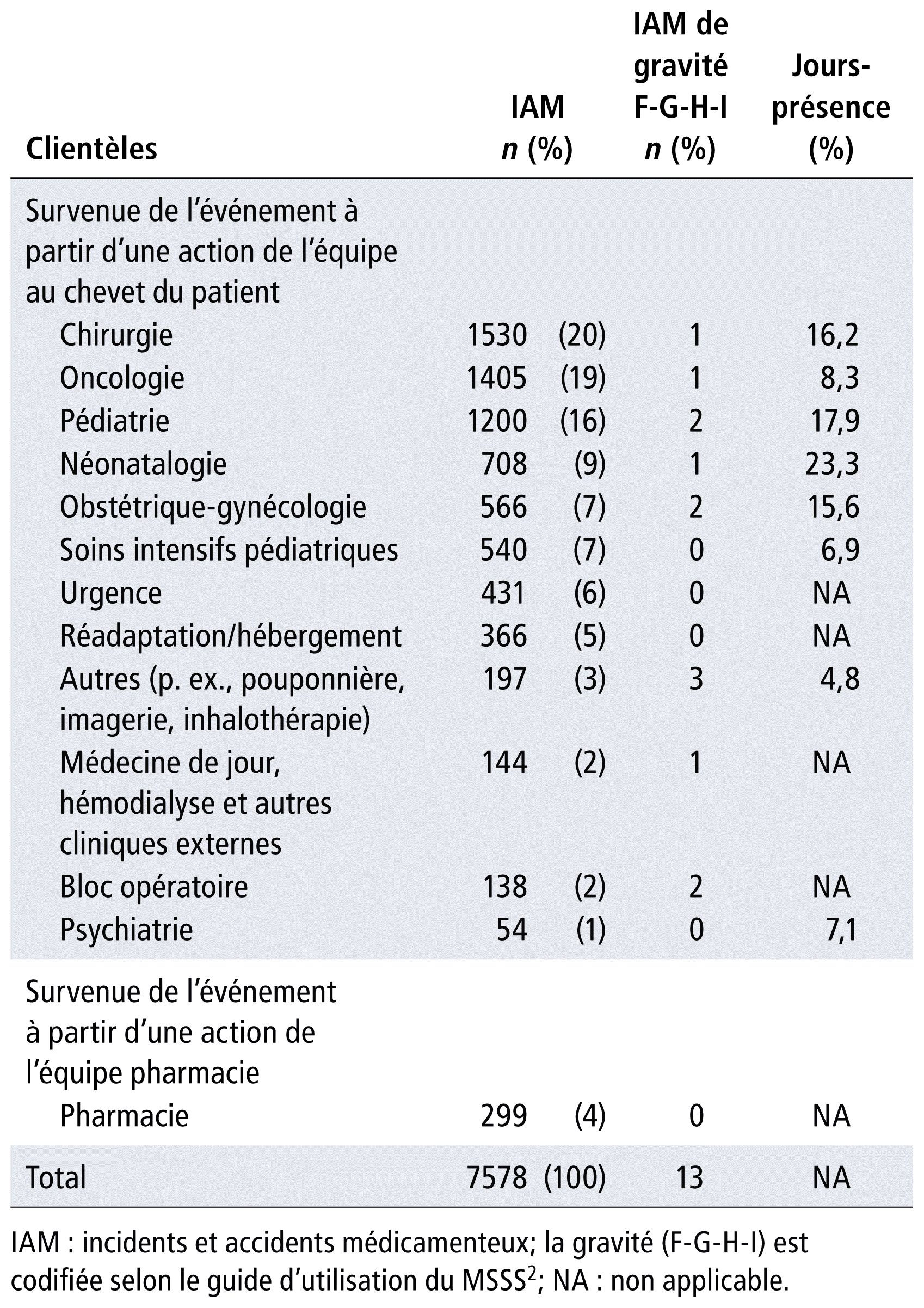
Le tableau 2 présente un profil du nombre d’IAM par clientèle en ordre décroissant.
TABLEAU 2 Profil du nombre d’IAM et de jours-présence par clientèle en ordre décroissant
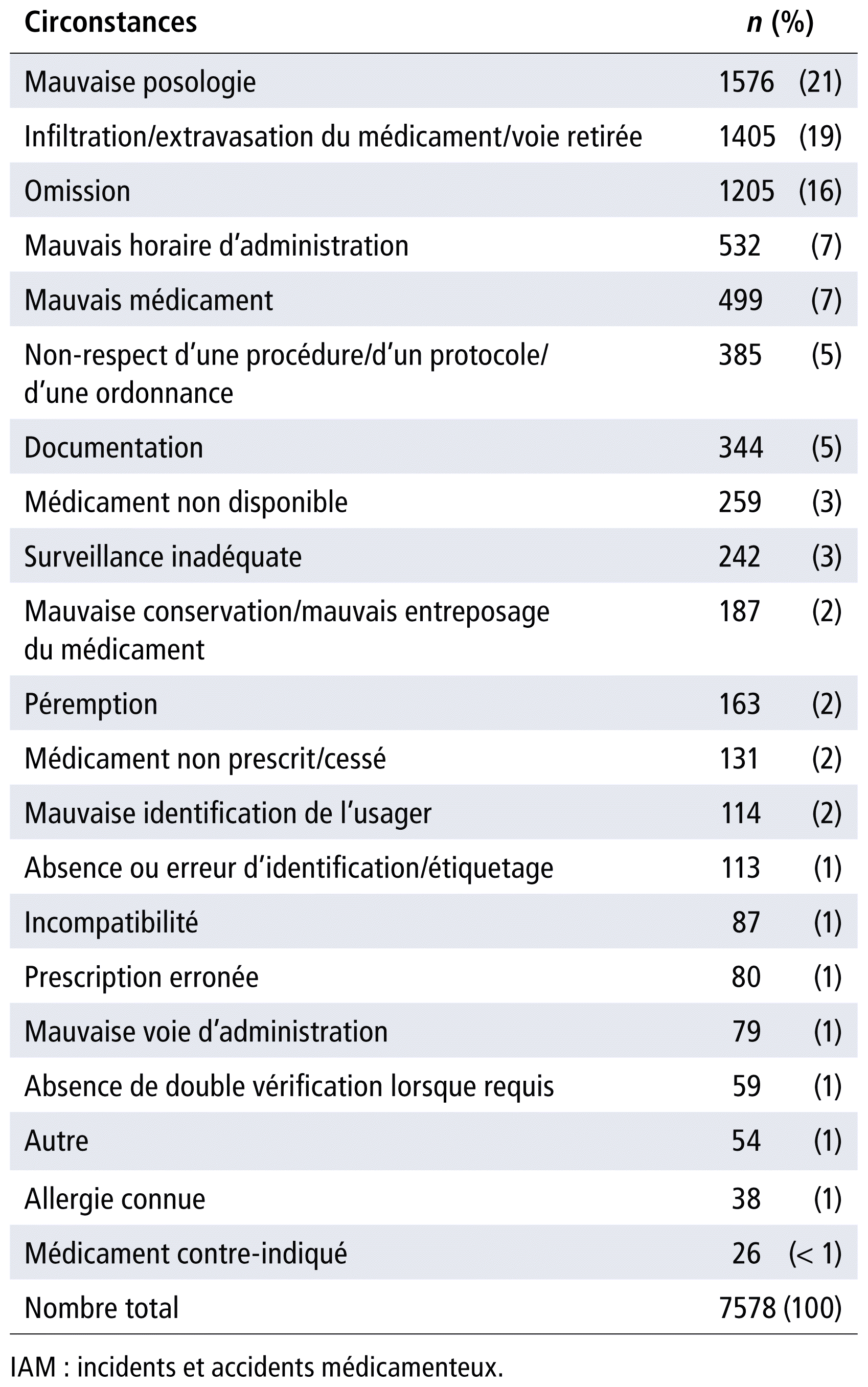
Des 21 circonstances rapportées, la plus fréquente était l’erreur de posologie (21 %, 1576/7578). Parmi ces erreurs, 67 % (1054/1576) concernaient un médicament administré par voie intraveineuse; 6 % (87/1576) étaient dues à des tubulures clampées; 4 % (59/1576) étaient liées à la prise en compte du poids du patient et 2 % (25/1576) étaient dues à une mauvaise dilution du médicament. En ce qui concerne les erreurs reliées à la voie intraveineuse, 26 % (270/1054) étaient dues à des erreurs de débit de soluté de base contre 9 % (95/1054) à des erreurs de débit des alimentations parentérales (AP).
La deuxième circonstance la plus fréquente était l’infiltration/extravasation/voie retirée (19 %, 1405/7578), ce qui se produit souvent chez les enfants.
La troisième circonstance la plus fréquente était l’omission de doses de médicaments (16 %, 1205/7578) (p. ex., patient absent lors de l’heure de prise prévue, erreurs de retranscription, médicament non administré par un tiers comme prévu).
Le tableau 3 présente un profil du nombre d’IAM par circonstance en ordre décroissant.
TABLEAU 3 Profil du nombre d’IAM par circonstance en ordre décroissant
Au total, 17 % (1265/7578) des IAM ont impliqué des solutés de base. Les IAM impliquant des solutés avec électrolytes étaient au nombre de 86 (1 %, 86/7578) dont 67 % (59/86) étaient des électrolytes concentrés. Le sulfate de magnésium était l’électrolyte concentré avec le plus grand nombre d’IAM (59 %, 35/59). Des erreurs portant sur le sulfate de magnésium, la majorité étaient de gravité mineure (33 sont de niveau A à D), 2 étaient de niveau de gravité E1.
Un total de 3 % (219/7578) d’IAM impliquaient des AP.
D’autres médicaments avaient un nombre absolu d’IAM important : acétaminophène (5 %, 339/7578), salbutamol (1 %, 85/7578), dexaméthasone (1 %, 68/7578), fentanyl (1 %, 48/7578), ibuprofène (1 %, 48/7578), intra-lipides (1 %, 47/7578), naproxène (1 %, 40/7578).
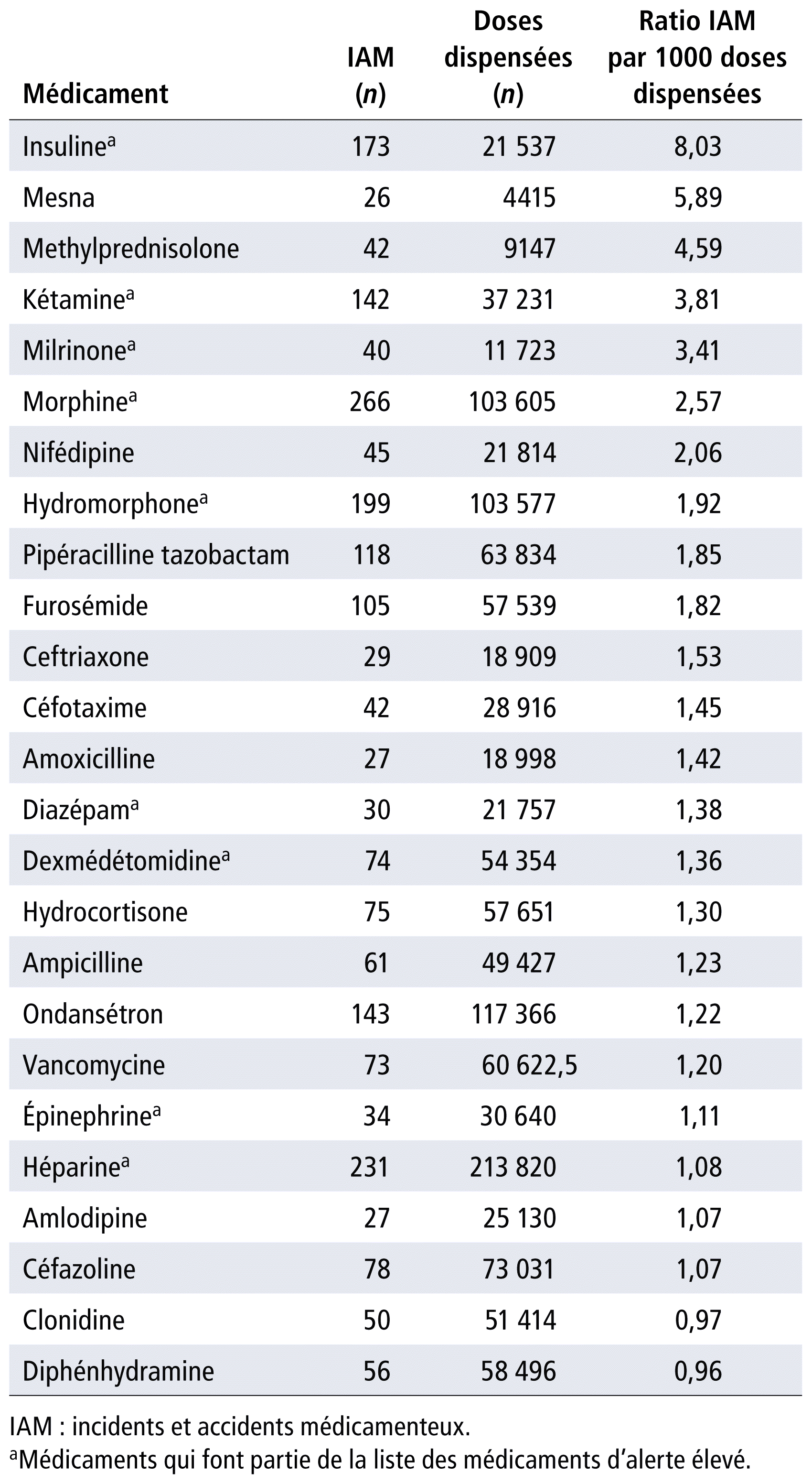
Le tableau 4 présente un profil du nombre d’IAM par 1000 doses dispensées en ordre décroissant pour une sélection de 25 médicaments. De cette liste, neuf médicaments font partie de la liste des médicaments d’alerte élevé et sont marqués d’un astérisque. De tous les IAM déclarés, 11 % (818/7578) étaient associés à des médicaments d’alerte élevée.
TABLEAU 4 Profil du nombre d’IAM par 1000 doses dispensées en ordre décroissant d’importance pour une sélection de 25 médicaments
En ce qui concerne le préjudice subi à la suite d’un IAM, des conséquences physiques étaient déclarées dans 15 % (1158/7578) des IAM. En revanche, des conséquences psychologiques étaient déclarées pour 1 % des IAM (44/7578).
La divulgation est obligatoire lorsque l’événement peut potentiellement avoir des conséquences. Du 1er avril 2018 au 31 mars 2021, elle était obligatoire pour les événements de gravité E1 à I. Dès le 1er avril 2021, elle est devenue obligatoire pour les événements de gravité D à I. Dans notre étude, lorsqu’elle était obligatoire, la divulgation était réalisée dans 99 % des cas (979/990).
En moyenne, le délai entre la date de l’événement et la date de saisie était de 52 jours.
Un panel d’experts composé d’un médecin, de quatre pharmaciens, de trois infirmières, de deux techniciens en pharmacie, d’une résidente en pharmacie et d’un gestionnaire de risque s’est réuni en avril 2023. Les observations des panélistes ont contribué aux recommandations suivantes : impliquer davantage les parents et les patients dans le circuit du médicament pour aider à la détection des événements; ajouter systématiquement les données d’IA, avec ratios lorsqu’applicable, dans les comités qualité et les réunions avec les soignants; éviter les ordonnances verbales et favoriser la saisie par le prescripteur électronique; limiter au minimum l’administration de doses de médicaments sans validation pharmaceutique, même si certaines doses sont disponibles dans les armoires automatisées; cibler davantage la diffusion des données d’IA liées aux événements de gravité F-G-H-I, en particulier avec les équipes médicales; s’assurer du bon usage des outils et technologies disponibles; encourager la déclaration et éviter que les ratios ne soient perçus comme des cibles de performance.
Cette étude descriptive présente un profil des IAM au sein d’un CHU du 1er avril 2018 au 31 mars 2022. Ce profil fait suite à deux analyses précédemment publiées7,8.
On observe une augmentation du nombre d’IAT et d’IAM par volume d’activités cliniques (c.-à-d. jour, admission, JP), mais pas par doses dispensées. Ainsi, le nombre moyen d’IAT déclaré/jour passe de 15 à 15,9 et le nombre d’IAM déclaré/jour passe de 4,7 à 5,2. Notre étude ne permet pas d’identifier un facteur particulier expliquant la hausse. On peut toutefois noter la présence d’une équipe de gestion des risques très proactive et l’utilisation courante de ces données par les équipes afin de comprendre et de réduire les risques d’IA au quotidien; une culture de déclaration est bien établie.
Ainsi, en dépit de la pandémie de COVID-19, le personnel soignant a maintenu la cadence dans la déclaration des IA. Toutefois, à l’échelle du Québec, il y a une diminution du nombre d’IAT déclarés (soit, 500 502 en 2018–2019, 495 652 en 2019–2020 contre 442 725 en 2020–2021), possiblement en lien avec les enjeux de la pandémie11–13. La pandémie de COVID-19 n’a touché les centres pédiatriques14 qu’à partir du printemps 2022.
Le nombre moyen d’IAM/1000 JP était de 22,4 dans notre établissement de 2018 à 2022, ce qui est plus élevé que la moyenne des CHU/Instituts (p. ex., moyenne de 11 ± 6 d’IAM/1000 JP en 2020–2021)15. Dans la littérature, plusieurs types de ratios sont utilisés. Par exemple, King et al. ont obtenu un ratio de 4,49 IAM/1000 JP dans un hôpital pédiatrique ontarien16. Manias et al. ont obtenu un ratio de 5,73 IAM/1000 JP dans un hôpital pédiatrique australien17. Walsh et al. ont obtenu un ratio de 48,2 IAM/1000 JP dans une sélection d’unités de soins pédiatriques, de soins intensifs pédiatriques et de soins intensifs néonataux18. Sakuma et al. ont obtenu un ratio de 65,1 IAM/1000 JP dans deux hôpitaux pédiatriques japonais19.
Plusieurs facteurs peuvent expliquer cette hétérogénéité, y compris la définition utilisée pour le numérateur (p. ex., incidents, accidents, incidents et accidents, effets indésirables aux médicaments). Le terme événement indésirable regroupe parfois les incidents/accidents et les effets indésirables aux médicaments20. Certaines études ne portent que sur les erreurs médicamenteuses17,18 tandis que d’autres portent sur les effets indésirables médicamenteux évitables, ou non16,19. L’OMS a établi des définitions de référence21. Certains pays, comme l’Australie, ont également mis en place un cadre consensuel pour standardiser les termes utilisés22. Au Québec, le MSSS a publié des lignes directrices6.
La culture de déclaration des IAT et des IAM au sein de l’établissement peut également expliquer ces différences. La proportion des erreurs déclarées peut varier d’un établissement à un autre. Une étude rapporte que seulement 57 % des erreurs médicamenteuses sont déclarées23.
Enfin, la population à traiter peut également expliquer ces différences. Aux États-Unis, environ 30 % des erreurs médicamenteuses se produisent en pédiatrie24. Les soins pédiatriques comportent davantage de risques compte tenu des médicaments prescrits selon le poids, du fait que les patients ne peuvent pas toujours s’exprimer et participer aux soins et à la détection des événements, du recours à davantage de préparations magistrales et davantage d’administration par voie intraveineuse nécessitant des dilutions ou reconstitutions et du recours aux prescriptions hors référentiels24,25.
La majorité des IAM surviennent de jour (34 %), puis de soir (29 %), de nuit (16 %) ou à un moment non renseigné (20 %). Dans notre pratique, l’infirmière de nuit (quart de 23 h 30 à 07 h 30) est responsable de réconcilier la feuille d’administration des médicaments avec les ordonnances en vigueur. Ce processus contribue à l’identification d’IA de façon rétrospective. Ces données n’étaient pas recueillies lors de l’étude de 2011–20188. Manias et al. et Gokhul et al. ont également noté que la majorité des erreurs surviennent de jour avec des proportions, respectivement, de 45 % et 52 % des erreurs survenant sur le quart de jour17,26.
On note une hausse de la proportion et du nombre d’événements de catégorie D, E1 et E2. Cette hausse est reliée à un changement de consigne de classification pour les infiltrations/extravasations depuis novembre 2020. Ainsi, la proportion d’IAM de gravité D est passée de 9 % en 2011–2018 à 17 % en 2018–2022. Les événements de gravité F-G-H-I restent très rares, soit 11 événements de 2011 à 2018 contre 13 événements de 2018 à 2022. Manias et al. ont codé la gravité selon une échelle de 1 à 8; d’après les définitions données, les erreurs de catégories 1 à 4 correspondent à un niveau de gravité de A à D. Ainsi, 97 % des erreurs rapportées par Manias et al. étaient de gravité A à D, ce qui est similaire à nos résultats, soit 99 % des IAM de catégorie A à D17.
En ce qui concerne les clientèles visées par les IAM, la majorité des IAM surviennent en chirurgie (20 %), en oncologie (19 %) et en pédiatrie (16 %). Ces proportions correspondent aux volumes d’activités en JP en chirurgie et en pédiatrie, mais pas en oncologie (19 % des IAM contre 8,3 % des JP). Sans surprise, l’oncologie comporte davantage de risques compte tenu des médicaments utilisés et du caractère tertiaire des soins prodigués. Manias et al. ont également identifié l’oncologie parmi les secteurs les plus à risque, avec les soins intensifs et les urgences17.
En ce qui concerne les circonstances associées aux IAM, la majorité des IAM est associée à une mauvaise posologie (21 %), des infiltrations/extravasations/voies retirées (19 %) et des omissions (16 %). Les circonstances varient selon les clientèles (p. ex., davantage de mauvaises posologies en oncologie et davantage d’infiltration/extravasation/voies retirées en chirurgie). Les circonstances associées à des événements plus graves sont relativement peu fréquentes (p. ex., médicament contre-indiqué (<1 %), allergie connue (1 %), mauvaise voie (1 %), incompatibilité (1 %), mauvaise identification de l’usager (2 %) à l’exception du mauvais médicament administré (7 %). Bratch et Pandit ont étudié les erreurs médicamenteuses en anesthésie et rapporté, parmi les erreurs les plus fréquentes, le recours au mauvais médicament et à la mauvaise dose, particulièrement en pédiatrie27. Bekes et al. ont noté que les causes d’une mauvaise posologie en anesthésie pédiatrique étaient les erreurs de dilution et les erreurs de calcul de dose28. Nos résultats sont en accord avec la littérature quant à la place dominante des erreurs de doses29.
En ce qui concerne le nombre d’IAM par 1000 doses dispensées, il varie de 0,96 à 8,03, avec plusieurs médicaments d’alerte élevée10. Il faut se questionner sur les pratiques lorsque le nombre absolu d’IAM est élevé. En revanche, il faut également cibler les IAM dont le ratio par 1000 doses dispensées est élevé. Dans la littérature, on retrouve peu d’études ayant examiné des ratios d’IAM par doses dispensées. Alghamdi et al. ont identifié, parmi quatre études menées en soins intensifs pédiatriques, les anti-infectieux, les agents cardiovasculaires et les sédatifs30. Greaney et al. ont calculé des ratios d’erreurs par 1000 doses d’opioïdes administrées et ont obtenu des ratios de 0,65 pour la morphine et de 0,36 pour l’hydromorphone31. Dans notre étude, les ratios par 1000 doses dispensées sont plus élevés (soit, 2,57 pour la morphine et 1,92 pour l’hydromorphone). Notre étude surestime les ratios parce que le dénominateur est utilisé comme si chaque format utilisé équivalait à une dose. De plus, la part des opioïdes est de 59,6 % dans l’étude de Greaney et al. contre seulement 10 % dans notre étude31.
Le recours à un panel d’experts est utile afin de commenter les données recueillies. Les sept suggestions formulées par le panel seront ramenées au comité central de la gestion des risques afin de bonifier les stratégies de prévention et d’intervention.
Cette étude comporte des limites. Elle ne porte que sur un établissement de santé québécois, mais elle offre une perspective longitudinale sur une démarche de gestion de risques. Elle ne présente que les IAT/IAM déclarés; le nombre réel d’événements demeure inconnu. Bien que les IAT/IAM soient déclarés sur un formulaire établi depuis longtemps, la codification reste imparfaite.
Cette étude descriptive rétrospective présente un profil des IA médicamenteux dans un CHU. L’étude offre un profil descriptif complet qui met en évidence la culture de déclaration des événements au sein de l’établissement et les éléments à prioriser pour limiter les risques pour la clientèle. Le partage de telles données favorise également l’analyse comparative avec d’autres établissements et peut contribuer aux échanges entourant la réduction des risques.
1 Organisation mondiale de la santé. Les médicaments sans les méfaits. S.d. [consulté le 11 juillet 2023]. Disponible à : https://www.who.int/fr/initiatives/medication-without-harm
2 Ministère de la santé et de services sociaux. Guide d’utilisation du rapport de déclaration d’incident ou d’accident. S.d. [consulté le 11 juillet 2023]. Disponible à : https://sptsss.com/media/PDF/AH-223.pdf
3 Bussières JF, Lebel D, Atkinson S, Tardif C, Meunier P. Le circuit du médicament en établissement de santé : une grille bonifiée pour mieux encadrer la formation des étudiants en pharmacie. Pharmactuel. 2021; 52(2):74–6.
4 LégisQuébec. Loi sur les services de santé et les services sociaux. Articles 183.1, 183.3, 183.4, 278, 391. 1991 [consulté le 11 juillet 2023]. Disponible à : https://www.legisquebec.gouv.qc.ca/fr/document/lc/s-4.2
5 Ministère de la santé et des services sociaux. Cadre de référence du registre national des incidents et accidents survenus lors de la prestation de soins de santé et de services sociaux. 2021 [consulté le 11 juillet 2023]. Disponible à : https://publications.msss.gouv.qc.ca/msss/fichiers/2021/21-735-02W.pdf
6 Ministère de la santé et des services sociaux. Déclaration des incidents et des accidents. Lignes directrices. S.d. [consulté le 11 juillet 2023]. Disponible à : https://publications.msss.gouv.qc.ca/msss/fichiers/2020/20-735-01W.pdf
7 Rochais E, Lebel D, Atkinson S, Rocheleau L, Bussières JF. Perspective sur les accidents et incidents médicamenteux en centre hospitalier universitaire. Risqu Qual Milieu Soins. 2011;8(4):243–52.
8 Chabrier A, Atkinson S, Lebel D, Bussières JF. Incidents et accidents médicamenteux en établissement de santé : analyse descriptive d’un CHU mère-enfant de 2011 à 2018. Risqu Qual. 2019;16(4):205–12.
9 Régie de l’assurance maladie du Québec. Liste des médicaments fournis en établissement. S.d. [consulté le 11 juillet 2023]. Disponible à : https://www.ramq.gouv.qc.ca/fr/a-propos/liste-medicaments-fournis-etablissement
10 Institute for Safe Medication Practices. Liste de médicaments de niveau d’alerte élevé. 2012 [consulté le 11 juillet 2023]. Disponible à : https://www.ismp-canada.org/fr/dossiers/HighAlertMedications2012_FR_3.pdf
11 Ministère de la santé et des services sociaux. Rapport 2018–2019 sur les incidents et accidents survenus lors de la prestation de soins de santé et de services sociaux – 1er avril 2018–31 mars 2019. 2019 [consulté le 11 juillet 2023]. Disponible à : https://publications.msss.gouv.qc.ca/msss/document-002445/
12 Ministère de la santé et des services sociaux. Rapport 2019–2020 sur les incidents et accidents survenus lors de la prestation de soins de santé et de services sociaux – 1er avril 2019–31 mars 2020. 2020 [consulté le 11 juillet 2023]. Disponible à : https://publications.msss.gouv.qc.ca/msss/document-002837/
13 Ministère de la santé et des services sociaux. Rapport 2020–2021 sur les incidents et accidents survenus lors de la prestation de soins de santé et de services sociaux – 1er avril 2020–31 mars 2021. 2021 [consulté le 11 juillet 2023]. Disponible à : https://publications.msss.gouv.qc.ca/msss/document-003233/
14 Pines JM, Zocchi MS, Black BS, Carlson JN, Celedon P, Moghatederi A, et al.; US Acute Care Solutions Research Group. Characterizing pediatric emergency department visits during the COVID-19 pandemic. Am J Emerg Med. 2021;41:201–4.
Crossref
15 Maurin C, Atkinson S, Hamouche L, Bussières JF. Ratios d’incidents et d’accidents médicamenteux par 1000 jours-présence en établissement de santé au Québec : une étude exploratoire [résumé]. Hopipharm 2023, 23–26 mai, Strasbourg, France.
16 King WJ, Paice N, Rangrej J, Forestell GJ, Swartz R. The effect of computerized physician order entry on medication errors and adverse drug events in pediatric inpatients. Pediatrics. 2003;112(3 Pt 1):506–9.
Crossref PubMed
17 Manias E, Cranswick N, Newall F, Rosenfeld E, Weiner C, Williams A, et al. Medication error trends and effects of person-related, environment-related and communication-related factors on medication errors in a paediatric hospital. J Paediatr Child Health. 2019;55(3):320–6.
Crossref
18 Walsh KE, Landrigan CP, Adams WG, Vinci RJ, Chessare JB, Cooper MR, et al. Effect of computer order entry on prevention of serious medication errors in hospitalized children. Pediatrics. 2008; 121(3):e421–7.
Crossref PubMed
19 Sakuma M, Ida H, Nakamura T, Ohta Y, Yamamoto K, Seki S, et al. Adverse drug events and medication errors in Japanese paediatric inpatients: a retrospective cohort study. BMJ Qual Saf. 2014; 23(10):830–7.
Crossref PubMed
20 Morimoto T, Gandhi TK, Seger AC, Hsieh TC, Bates DW. Adverse drug events and medication errors: detection and classification methods. Qual Saf Health Care. 2004;13(4):306–14.
Crossref PubMed PMC
21 Organisation mondiale de la santé. Conceptual framework for the international classification for patient safety. Final technical report. 2009 janvier [consulté le 11 juillet 2023] Disponible à : https://apps.who.int/iris/bitstream/handle/10665/70882/WHO_IER_PSP_2010.2_eng.pdf
22 Australian Commission on Safety and Quality in Healthcare. Classification of prescribing and medicine administration adverse events and incidents. [consulté le 11 juillet 2023]. Disponible à : https://www.safetyandquality.gov.au/publications-and-resources/resource-library/classification-prescribing-and-medicine-administration-adverse-events-and-incidents
23 Jember A, Hailu M, Messele A, Demeke T, Hassen M. Proportion of medication error reporting and associated factors among nurses: a cross sectional study. BMC Nurs. 2018;17:9.
Crossref PubMed PMC
24 Wu, A. Minimizing medication errors in pediatric patients. US Pharm. 2018;44:20–3.
25 Conn RL, Kearney O, Tully MP, Shields MD, Dornan T. What causes prescribing errors in children? Scoping review. BMJ Open. 2019;9(8):e028680.
Crossref PubMed PMC
26 Gokhul A, Jeena P, Gray A. Iatrogenic medication errors in a paediatric intensive care unit in Durban, South Africa. S Afr Med J 2016;106: 1222–9.
Crossref PubMed
27 Bratch R, Pandit JJ. An integrative review of method types used in the study of medication error during anaesthesia: implications for estimating incidence. Br J Anaesth. 2021;127(3):458–69.
Crossref PubMed
28 Bekes JL, Sackash CR, Voss AL, Gil CJ. Pediatric medication errors and reduction strategies in the perioperative period. AANA J. 2021; 89(4):319–24.
PubMed
29 Gates PJ, Meyerson SA, Baysari MT, Westbrook JI. The prevalence of dose errors among paediatric patients in hospital wards with and without health information technology: a systematic review and meta-analysis. Drug Saf. 2019;42(1):13–25.
Crossref
30 Alghamdi AA, Keers RN, Sutherland A, Ashcroft DM. Prevalence and nature of medication errors and preventable adverse drug events in paediatric and neonatal intensive care settings: a systematic review. Drug Saf. 2019;42(12):1423–36.
Crossref PubMed PMC
31 Greaney D, Roy R, McDonnell C. Opioid-related harm in a quaternary pediatric hospital: a 5-year review. J Opioid Manag. 2020;16(5):375–82.
Crossref PubMed
Adresse de correspondance: Jean-François Bussières, CHU Sainte-Justine, 3175, chemin de la Côte Sainte-Catherine, Montréal QC H3T 1C5, Courriel: jean-francois.bussieres.hsj@ssss.gouv.qc.ca
Conflits d’intérêts: Aucun
Financement: Aucun reçu.
Soumis: 21 juillet 2023
Accepté: 11 octobre 2023
Publié: 10 avril 2024
© 2024 Canadian Society of Hospital Pharmacists | Société canadienne des pharmaciens d’hôpitaux
Canadian Journal of Hospital Pharmacy, VOLUME 77, NUMBER 2, 2024